Pourquoi préserver sa fertilité ?
Traitements
Certains traitements ou interventions chirurgicales peuvent, en raison de leurs effets secondaires, avoir pour conséquence une diminution ou un arrêt de la production des spermatozoïdes chez l’homme ou des ovocytes chez la femme et donc présenter un risque pour une fertilité immédiate ou future.
Cet arrêt de la production peut être transitoire ou définitif en fonction du type de traitement. Cela se produit le plus souvent pour les traitements du cancer. Mais dans certains cas, des médicaments ou des interventions chirurgicales employés pour des maladies non cancéreuses peuvent également présenter un risque pour la fertilité. Les médecins qui vous suivent ainsi que nos équipes médicales peuvent vous apporter toute information sur l’existence de risques pour la fonction de reproduction.
Contexte
Dans ce contexte la préservation de la fertilité est en général possible et fait appel à des méthodes spécifiques qui doivent être mises en place avant de débuter les traitements. Les CECOS sont disponibles très rapidement pour répondre à la demande des patients et de leur médecins.
La congélation cellulaire à des fins de préservation consiste à protéger et conserver par refroidissement des cellules, qui peuvent être issues de différents tissus. Ces cellulles sont maintenues dans un état de vie et d’animation suspendues à des tempéraures dites cryogéniques dans l’azote liquide (-196°C) ou dans les vapeurs d’azote (-140°C). Ces procédues de congélation cellulaire sont utilisées chez l’homme et la femme pour conserver les gamètes (ovocytes et spermatozoïdes), les embryons ou les tissus germinaux (ovaire ou testicule)en vue d’une utilisation ultérieure dans le cadre d’une assistance médicale à la procréatin (AMP).
La préservation médicale de la fertilité féminine
Pourquoi préserver la fertilité feminine ?
Une augmentation de 89% du nombre de cas de cancer a été observée en France entre 1980 et 2005. A partir de 2005, on note une diminution du taux d’incidence chez l’homme et une stabilisation chez la femme.
Cependant, la survie après un traitement du cancer s’est considérablement améliorée au cours des 30 dernières années du fait de l’amélioration du diagnostic et de l’efficacité des traitements.
Chez la femme, en 2016, le taux de survie à 5 ans, tous cancers confondus est de 66 %.
L’augmentation de l’efficacité des traitements du cancer s’accompagne d’une augmentation de leur toxicité. Les séquelles ne sont pas exceptionnelles chez les patients guéris d’un cancer. Les gonades sont une cible de choix de cette toxicité et ainsi les cellules primitives (ovocytes immatures).
Ainsi, l’ovaire peut être atteint à la fois au niveau endocrine (follicules ovariens) et de sa fonction exocrine (élaboration des gamètes matures de type ovocytes II).
Le traitement du cancer peut retentir sur la fertilité future de la patiente du fait non seulement de la toxicité propre du traitement sur la réserve ovarienne en follicules primordiaux mais aussi du report de la grossesse induit par la durée du traitement et de la surveillance post-thérapeutique nécessaire pour autoriser la grossesse.
En dehors du cancer, des traitement médicamenteux gonadotoxiques (agents alkylants, certains traitements immunosuppresseurs …) peuvent être proposés dans les maladies hématologiques non malignes, les maladies du système immunitaire. Les pathologies bénignes imposant un geste chirurgical peuvent avoir un retentissement sur la fertilité future de la femme. Enfin, les atteintes congénitales de la gonade, le plus souvent d’origine génétique, peuvent altérer prématurément la production de gamètes matures entraînant une insuffisance ovarienne prématurée chez la femme.
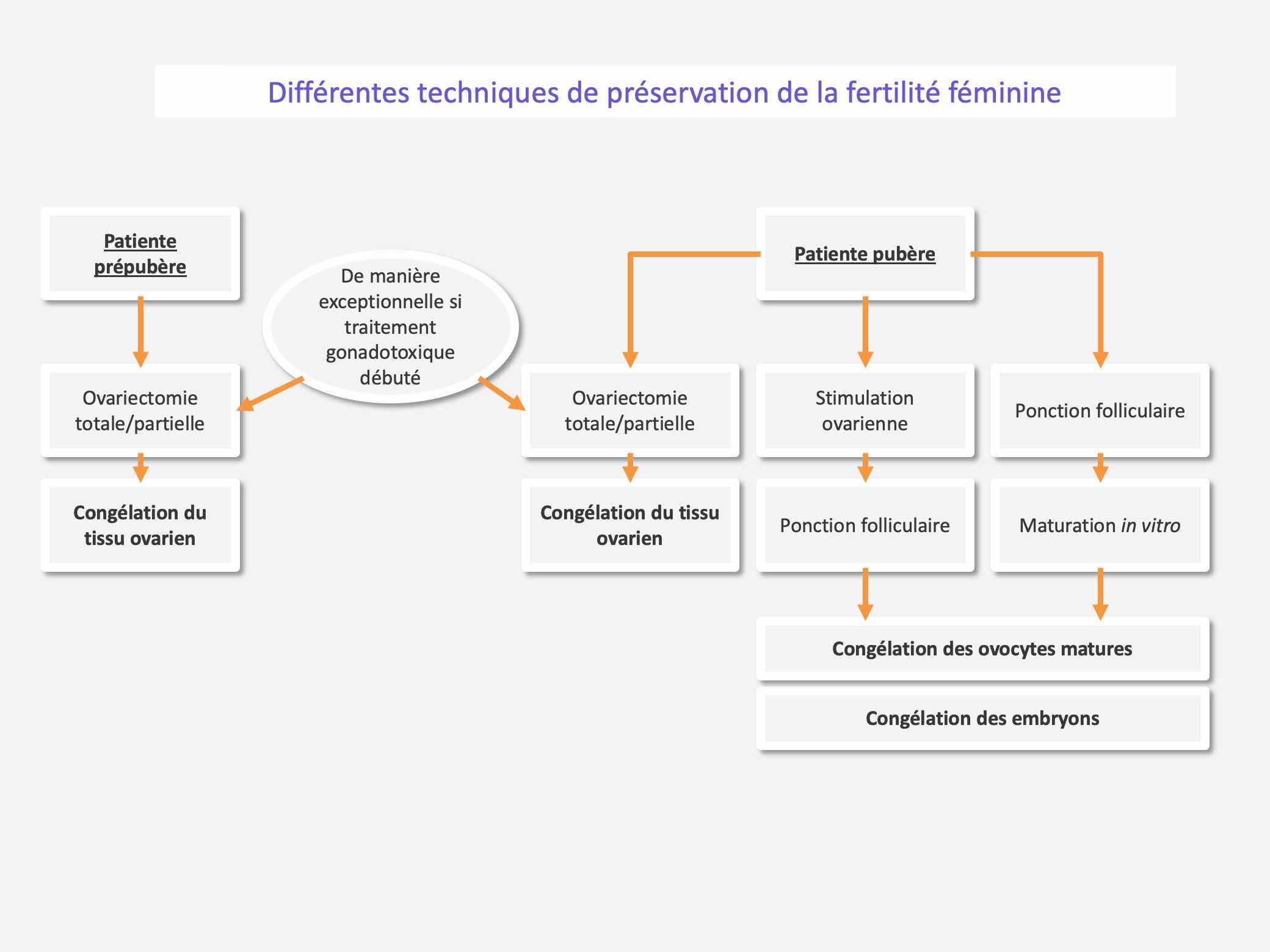
Techniques de préservation du potentiel de la fertilité féminine
Chez la femme, différentes techniques de préservation du potentiel de la fertilité sont envisageables de manière isolée ou associée : la congélation d’ovocytes, la congélation d’embryons et la congélation du tissu ovarien.
C’est la technique la plus récente de préservation du potentiel de la fertilité fémnine.
Elle s’est largement développée depuis l’utilisation de la technique de vitrification ovocytaire qui améliore considérablement la survie des ovocytes après décongélation et les chances de grossesses après fécondation in vitro.
Cette procédure est réservée aux femmes pubères, en couple ou célibataires. Elle s’effectue préférentiellement à partir d’ovocytes matures, obtenus dans la majorité des cas après stimulation de l’ovulation ou plus exceptionnellement après maturation in vitro.
La congélation d’ovocytes immatures peut parfois être proposée en complément de la congélation d’ovocytes matures, pour les ovocytes qui ne sont pas matures au moment de la congélation.
Cette méthode nécessite un recueil d’ovocytes matures, uniquement réalisable chez une patiente pubère qui peut subir une stimulation hormonale de l’ovulation avant la réalisation d’un traitement gonadotoxique.
Cette technique implique l’existence d’un conjoint et d’un projet parental.
Elle constitue une procédure de préservation du potentiel de la fertilité du couple et non de la femme, les embryons conservés ne pouvant être utilisés qu’au sein du couple.
Cette technique a pour but de conserver des follicules ovariens primordiaux situés dans le cortex ovarien.
Cette technique est envisageable chez la femme avant et après la puberté. Elle ne nécessite pas de stimulation de l’ovulation et peut être proposée lorsqu’un traitement faiblement gonadotoxique a été débuté.
La procédure de congélation du tissu ovarien débute par le prélèvement d’un ovaire entier ou de fragments biopsiques de cortex ovarien.
L’intervention est soit réalisée, habituellement par coelioscopie, spécifiquement pour le prélèvement chirurgical de l’ovaire, soit le plus souvent associée à un geste chirurgical de l’ovaire dans le contexte de la maladie (mise en place d’un chambre implantatoire ou d’un cathéter central, résection d’une masse tumorale …).
L’utilisation via la greffe orthotopique de fragments de tissu ovarien congelé restaure la fonction ovarienne endocrine de la femme et a déjà permis la naissance de plus d’une centaine d’enfants dans le monde.
La congélation de tissu ovarien est la seule technique possible chez la jeune fille prépubère et l’enfant. Chez la femme pubère, les différentes techniques peuvent être associées, si cela s’avère possible.
La préservation médicale de la fertilité masculine
L’augmentation de l’efficacité des traitements du cancer s’accompagne d’une augmentation de leur toxicité. Les complications ou les séquelles ne sont pas exceptionnelles chez les patients guéris d’un cancer.
Ces séquelles sont extrêmement variables dans leur type, leur intensité et leur retentissement sur la qualité de vie, parmi lesquelles on citera les altérations de la fonction de reproduction, bien souvent oubliées comme séquelles éventuelles de ces traitements. En effet, les gonades constituent une cible de choix de cette toxicité, le testicule étant plus vulnérable que l’ovaire.
La cellule germinale immature est la cellule cible de cette toxicité : spermatogonies souches dans les tubes séminifères chez l’homme. Ainsi, la gonade (testicule) peut-être atteinte à la fois au niveau de sa fonction endocrine (cellules de Leydig) mais aussi sa fonction exocrine [élaboration des gamètes matures (spermatozoïdes).
Les effets toxiques des traitements sur la gonade et leur intensité vont dépendre du type de traitement utilisé (radiothérapie, chimiothérapie, chirurgie de la gonade, biothérapie, hormonothérapie…), de la dose cumulée reçue et de leur durée. Indépendamment de ces paramètres, le facteur individuel – qui correspond (i) soit à la fonctionnalité de la gonade au moment du traitement, soit à une sensibilité plus importante de celle-ci à l’effet toxique des traitements – est souvent plus difficile à évaluer.
En savoir plus
Chez l’homme, le traitement du cancer aura pour conséquence une diminution plus ou moins importante de la production de spermatozoïdes qui pourra conduire à une azoospermie non obstructive pour les traitements les plus toxiques (agents alkylants à forte dose, radiothérapie testiculaire directe, chimiothérapie et/ou radiothérapie avant allo- ou autogreffe de cellules souches hématopoïétiques). La fonction endocrine est plus exceptionnellement altérée. La chirurgie du cancer peut également altérer la fertilité de l’homme, comme l’orchidectomie uni- ou bilatérale pour traiter le cancer du testicule ou toute intervention chirurgicale susceptible d’entraîner une anéjaculation ou éjaculation rétrograde voire des troubles de l’érection comme la prostatectomie radicale et certains curages ganglionnaires rétro-péritonéaux.
Des traitements médicamenteux gonadotoxiques (agents alkylants, certains traitements immunosuppresseurs…) peuvent également être proposés hors champ du cancer par exemple dans les pathologies hématologiques non malignes, les maladies du système immunitaire …. Il peut s’agir d’une préservation de la fertilité réalisée avant allo- ou autogreffe de cellules souches hématopoïétiques. La chirurgie gonadique est une indication au recours aux techniques de préservation de la fertilité. Enfin, les atteintes congénitales de la gonade, le plus souvent d’origine génétique, peuvent altérer prématurément la production de gamètes matures responsables d’une perte prématurée des spermatogonies souches entrainant une azoospermie non obstructive chez l’homme.
De manière plus spécifique chez l’homme après la puberté, la préservation de la fertilité est ainsi proposée hors champ du cancer : avant toute intervention chirurgicale susceptible d’entraîner une anéjaculation ou éjaculation rétrograde : résection transuréthrale de la prostate, intervention sur le col de la vessie, avant stérilisation chirurgicale à visée contraceptive (vasectomie), en cas d’intervention chirurgicale sur les testicules ou les voies excrétrices spermatiques : tumeur testiculaire bénigne, traitement chirurgical de l’orchi-épididymite, torsion testiculaire, cure de cryptorchidie tardive, choc testiculaire, cure de varicocèle, après recueil chirurgical de spermatozoïdes dans les voies excrétrices spermatiques dans les azoospermies obstructives ou par biopsie chirurgicale testiculaire dans les azoospermies non obstructives, en cas d’altérations spermatiques susceptibles de s’aggraver au cours du temps et pouvant conduire à une azoospermie non obstructive (oligozoospermie sévère, dégradation des paramètres spermatiques au cours de la prise en charge en AMP, syndrome de Klinefelter, microdélétion du chromosome Y…).
Chez l’homme avant la puberté, deux autres indications plus exceptionnelles de préservation de la fertilité, en dehors du contexte de l’allo- ou autogreffe de cellules souches hématopoïétiques, sont représentées par les garçons pré-pubères ou adolescents présentant un syndrome de Klinefelter ou les garçons pré-pubères avec une cryptorchidie, la préservation de la fertilité étant pratiquée lors de l’orchidopexie du testicule de façon uni- ou bilatérale.
Techniques de préservation de la fertilité masculine
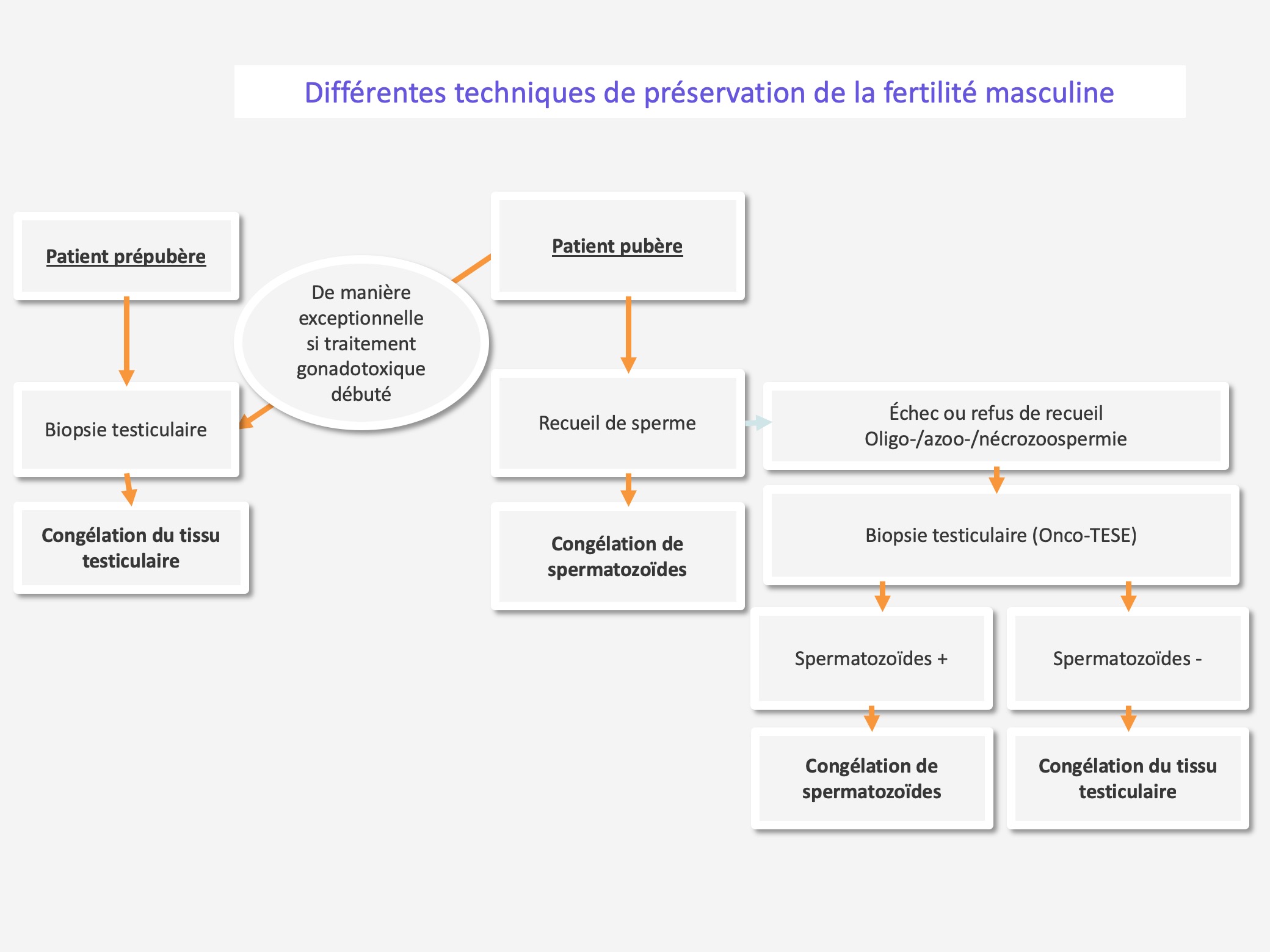
Congélation de spermatozoïdes
Chez l'homme pubère
Chez l’homme pubère (adolescent ou adulte), il est théoriquement possible d’effectuer une congélation de spermatozoïdes obtenus après un recueil de sperme par masturbation, dès le stade III de Tanner avec un volume testiculaire supérieur à 5mL. Néanmoins, en cas d’échec ou de refus de recueil de spermatozoïdes, d’oligozoospermie sévère, d’azoospermie ou de nécrozoospermie, une procédure alternative consiste à envisager la biopsie testiculaire avec extraction de spermatozoïdes (Onco-TESE) suivie de leur congélation. Cette Onco-TESE, si elle s’avère négative, peut être associée à la congélation d’une partie du tissu testiculaire, afin de pouvoir conserver des cellules souches spermatogoniales (CSS) si elles sont présentes. La congélation de spermatozoïdes doit être effectuée avant la mise en route du traitement gonadotoxique pour éviter dans le cas de la chimiothérapie ou radiothérapie l’effet mutagène sur les spermatozoïdes avec un risque potentiel si utilisation dans le cadre d’une AMP sur le conceptus (fausses-couches, malformations, anomalies génétiques ou chromosomiques). Les spermatozoïdes éjaculés conservés seront utilisables selon les différentes techniques d’AMP (insémination, FIV ou fécondation in vitro avec microinjection [ICSI]) en fonction du nombre et de la mobilité des spermatozoïdes après décongélation. Les spermatozoïdes issus de TESE sont uniquement utilisables en ICSI. La majorité des conservations de spermatozoïdes s’effectue dans le champ du cancer, principalement avant traitement du cancer du testicule, du lymphome malin Hodgkinien ou non Hodgkinien et des tumeurs solides.
Chez le garçon prébubère ne produisant pas de spermatozoïdes
Chez le garçon pré-pubère ne produisant pas de spermatozoïdes ou le garçon pubère ayant déjà initié son traitement gonadotoxique (chimiothérapie ou radiothérapie) à dose faiblement toxique et n’ayant pas eu la possibilité de conserver ses spermatozoïdes préalablement, l’Onco-TESE n’a pas sa place. Dans la seconde situation, les spermatozoïdes qui sont produits ont subi l’effet mutagène des traitements et ne sont pas utilisables en AMP. La biopsie testiculaire associée à la congélation de fragments de tissu testiculaire semble être une solution acceptable, avec pour objectif, une préservation des CSS. Il est bien entendu important d’informer les patients et leurs parents si mineurs que la possible utilisation ultérieure du tissu testiculaire congelé reste à l’heure actuelle du domaine de la recherche. En effet, les différentes modalités d’utilisation envisageables sont actuellement développées sur les modèles animaux, à savoir la maturation in vitro des cellules germinales souches isolées ou maintenues au sein du tissu testiculaire afin de produire in vitro des spermatozoïdes, la transplantation des cellules germinales souches ou la greffe du tissu testiculaire afin de produire in vivo des spermatozoïdes chez le patient guéri. Les spermatozoïdes produits in vitro ou in vivo seraient utilisables dans le cadre d’une ICSI. La majorité des conservations de tissu testiculaire s’effectue dans le champ du cancer avant allogreffe de CSH dans le cadre des leucémies aigües ou autogreffe de CSH dans le cadre des lymphomes ou tumeurs du système nerveux central.
En pratique :
Tout patient devant bénéficier d’une cryoconservation doit prendre un rendez-vous dans un laboratoire ayant l’autorisation pour congeler et conserver le sperme.
La conservation devra se faire avant de débuter le traitement et/ou avant l’intervention chirurgicale.
Le patient sera reçu par un des praticiens du CECOS et les informations concernant la congélation, la conservation et l’utilisation ultérieure des paillettes lui seront données.
Un dossier spécifique sera ouvert comprenant :
- résultat des sérologies suivantes (datant de moins de 6 mois) : HIV 1et2, Hépatite B, Hépatite C et Syphilis
- consentement et contrat signés
- pièce d’identité du patient
En cas d’autoconservation de sperme en urgence, tout sera mis en œuvre pour connaître le statut sérologique (dépistage des maladies infectieuses) avant le traitement et le conditionnement du sperme au laboratoire.
Le sperme est recueilli par auto-masturbation au CECOS, il est recommandé, quand cela est possible, de respecter auparavant un délai d’abstinence sexuelle de 2 à 7 jours.
En général, afin de conserver une quantité suffisante de sperme, le patient peut être amené à réaliser deux à trois prélèvements. Le praticien du centre informera le patient de la qualité de la conservation.
Dans certains cas particuliers (atteinte de la moelle épinière, paraplégie, masturbation non effective….) le prélèvement de sperme peut être obtenu par l’usage d’un vibromasseur médical ou plus exceptionnellement dans certains centres par électro-éjaculation.
Avant toute congélation, le sperme sera analysé (volume du sperme, concentration, mobilité et vitalité des spermatozoïdes). Pour être congelé, le sperme doit être mélangé à un cryoprotecteur avant d’être conditionné dans des paillettes dites Haute Sécurité de 0,3 ml . Chacune de ces paillettes sera identifiée à l’aide d’un numéro attribué à chaque patient. Elles seront ensuite congelées à l’aide d’un congélateur automatisé avec une descente progressive en température. Le stockage des paillettes se fera dans l’azote liquide à – 196°C .
Une fois congelé, le sperme peut être conservé aussi longtemps que le patient le désire sans altération du pouvoir fécondant.
Chaque année, le patient recevra un courrier lui demandant s’il souhaite poursuivre ou non la conservation de ses paillettes de sperme. En cas de déménagement, il est important de donner sa nouvelle adresse au CECOS qui conserve vos paillettes.
En cas de projet parental, il sera possible d’utiliser les paillettes congelées après réévaluation des paramètres spermatiques. Cette utilisation se fera en Assistance Médicale à la Procréation. L’équipe du CECOS vous accompagnera si besoin dans cette démarche.
Il est tout à fait possible de transférer vos paillettes de sperme d’un CECOS à l’autre. Le médecin du centre qui conserve vos paillettes remettra au centre qui réceptionnera vos paillettes un compte rendu comprenant le nombre de paillettes transférées ainsi que leur qualité. Le transfert sera à votre charge. Un container pour transporter les paillettes pourra vous être loué par un des 2 centres.
La préservation de la fertilité chez l’enfant et l’adolescent
Chez les enfants et adolescents, le cancer touche chaque année, en moyenne 2200 nouvelles personnes (1750 chez les moins de 15 ans et 450 chez les adolescents de 15 à 19 ans en 2015)*.
La survie à 5 ans des enfants et adolescents atteints de ces cancers s’est améliorée de manière très significative ces dernières décennies et dépasse aujourd’hui 80%.
La préservation du potentiel de la fertilité future prend donc une importance toute particulière dans cette population et chez d’autres jeunes patient(e)s devant recevoir un traitement potentiellement stérilisant en dehors d’une maladie cancéreuse.
L’information des jeunes patient(e)s et de leurs parent au sujet des conséquences des traitements sur la fertilité est recommandée, quelque soient leur origine, leur religion, leur culture, leur statut socioéconomique ou leur orientation sexuelle.
Les équipes des CECOS sont sensibilisées et formées à recevoir de jeunes patient(e)s ainsi que leurs parents afin de leur délivrer une information et un accompagnement à la préservation du potentiel de la fertilité tout en tenant compte des spécificités des jeunes enfants et adolescents.
Le consentement des parents est obligatoire mais l’avis du jeune patient(e) quelque soit son âge est pris en compte dans la discussion et la décision.
Le CECOS c'est quoi ?
Des plaquettes d’information spécifiques sont disponibles : « le CECOS c’est quoi » et plaquettes ligne nationale contre le cancer.
Que la préservation de la fertilité ait pu aboutir, ou pas, un suivi des jeunes patient(e)s est proposé par les équipes des CECOS en lien avec les services d’oncologie, pédiatrie, endocrinologie, gynécologie et andrologie. A leur majorité, les jeunes patient(e)s sont systématiquement convoqués en consultation multidisciplinaire.
Une évaluation de la fertilité à distance des traitements est proposée et une deuxième phase de préservation peut être proposée dans certain cas.
Les techniques de préservation envisageables pour les enfants et adolescents sont décrites dans les chapitres « préservation de la fertilité féminine » et « préservation de la fertilité masculine »
*chiffres issus de l’Institut National du Cancer (INCa)
Lors d’une transition de genre
Lors d’un parcours de transition de genre (Femme vers Homme, Homme vers Femme ou autres parcours de personnes non-binaires) les traitements hormonaux et/ou chirurgicaux peuvent avoir un impact sur le potentiel de fertilité future.
Les recommandations françaises (HAS 2009), et internationales (WPATH Version 8 2022), précisent qu’une information sur les possibilités de préservation de la fertilité doit être donnée aux personnes en cours de transition de genre.
Ainsi, depuis mai 2018, la fédération des CECOS a émis un consensus pour la prise en charge des personnes entamant un parcours de transition ou en cours de transition afin de les informer sur les possibilités de préservation de leur potentiel de fertilité, et de proposer en fonction du contexte la conservation de gamètes (spermatozoïdes et ovocytes), ou de tissus germinaux.
Au regard de la loi de Bioéthique actuelle, les utilisations en France sont difficiles mais l’évolution potentielle de la loi nous incite à anticiper les possibilités d’utilisation des gamètes au cours d’une assistance médicale à la procréation (AMP). L’utilisation éventuelle des tissus germinaux soulève des questionnements qui ne trouvent pas encore de réponses dans les techniques d’AMP actuelles.
Les centres CECOS reçoivent donc les personnes transidentitaires souhaitant une information sur la préservation de la fertilité. Les possibilités de conservation des gamètes (spermatozoïdes et/ou ovocytes) voire des tissus germinaux ne sont pas disponibles dans tous les centres, mais un réseau est présent et permettra une prise en charge de proximité.
Lors d’une préservation non médicale
CE QUE DIT LA LOI
« Art. R. 2141-37. – Les conditions d’âge requises par l’article L. 2141-12 pour bénéficier de
l’autoconservation de ses gamètes en vue de la réalisation ultérieure d’une assistance médicale à la procréation
sont fixées ainsi qu’il suit :
« 1. Le prélèvement d’ovocytes peut être réalisé chez la femme à compter de son vingt-neuvième anniversaire et
jusqu’à son trente-septième anniversaire ;
« 2. Le recueil de spermatozoïdes peut être réalisé chez l’homme à compter de son vingt-neuvième anniversaire
et jusqu’à son quarante-cinquième anniversaire.
Suite aux modifications des lois de bioéthique et l’édition de la loi du 02 aout 2021, la préservation de fertilité non médicale est désormais autorisée.
CHEZ LA FEMME
Chez la Femme, la préservation de fertilité non médicale est possible de 29 à 37 ans. Cela consiste en une stimulation ovarienne suivi d’une ponction folliculaire afin de recueillir des ovocytes matures. Ces ovocytes matures seront ensuite congelés/vitrifiés au CECOS pour un usage ultérieur, dans le cadre d’une technique d’AMP.
Chaque année, vous recevrez un courrier vous demandant la poursuite ou non de la conservation des ovocytes ainsi qu’une facture anuelle de 40.50 euros correspondant aux frais de conservation des ovocytes. En cas de déménagement, il est important de donner votre nouvelle adresse au CECOS qui conserve vos paillettes.
En cas de projet parental, il sera possible d’utiliser vos ovocytes congelés. Cette utilisation se fera en Assistance Médicale à la Procréation. L’équipe du CECOS vous accompagnera si besoin dans cette démarche. L’utilisation de vos ovocytes est possible jusqu’à votre 45ème anniversaire.
Il est tout à fait possible de transférer vos paillettes d’ovocytes d’un CECOS à l’autre. Le médecin du centre qui conserve vos ovocytes remettra au centre qui les réceptionnera un compte rendu de la tentative. Le transfert sera à votre charge. Un container pour transporter les paillettes pourra vous être loué par un des 2 centres.
Si vous avez plus de 45 ans ou si vous n’avez plus de projet parental, vous avez la possibilité de faire un don de vos ovocytes.
Les délais d’attente pour une première ponction folliculaire peuvent varier d’un centre à un autre.
CHEZ L’HOMME
Chez l’homme, la préservation de fertilité non médicale est possible de 29 à 45 ans. Cela consiste à réaliser un ou plusieurs prélèvements de spermatozoïdes au CECOS. Les spermatozoïdes seront alors congelés pour un usage ultérieur, dans le cadre d’une technique d’AMP.
Chaque année, vous recevrez un courrier vous demandant la poursuite ou non de la conservation de vos spermatozoïdes ainsi qu’une facture anuelle de 40.50 euros correspondant aux frais de conservation des spermatozoïdes. En cas de déménagement, il est important de donner votre nouvelle adresse au CECOS qui conserve vos paillettes.
En cas de projet parental, il sera possible d’utiliser vos spermatozoïdes congelés. Cette utilisation se fera en Assistance Médicale à la Procréation. L’équipe du CECOS vous accompagnera si besoin dans cette démarche. L’utilisation de vos paillettes est possible jusqu’à votre 60ème anniversaire.
Il est tout à fait possible de transférer vos paillettes de spermatozoïdes d’un CECOS à l’autre. Le médecin du centre qui conserve vos spermatozoïdes remettra au centre qui les réceptionnera un compte rendu du prélèvement. Le transfert sera à votre charge. Un container pour transporter les paillettes pourra vous être loué par un des 2 centres.
Si vous avez plus de 60 ans ou si vous n’avez plus de projet parental, vous avez la possibilité de faire un don de vos spermatozoïdes.
Pour plus d’informations, contactez le CECOS le plus proche de chez vous : annuaire des CECOS
Siège social
478 Rue de la Découverte
Mini Parc 3
CS 67624 31676 LABEGE Cedex
SIREN 300 089 646
SIRET 300 089 646 00032
Déclaration Activité N° 76 31 09316 31
Code APe 7219Z
Nous contacter





